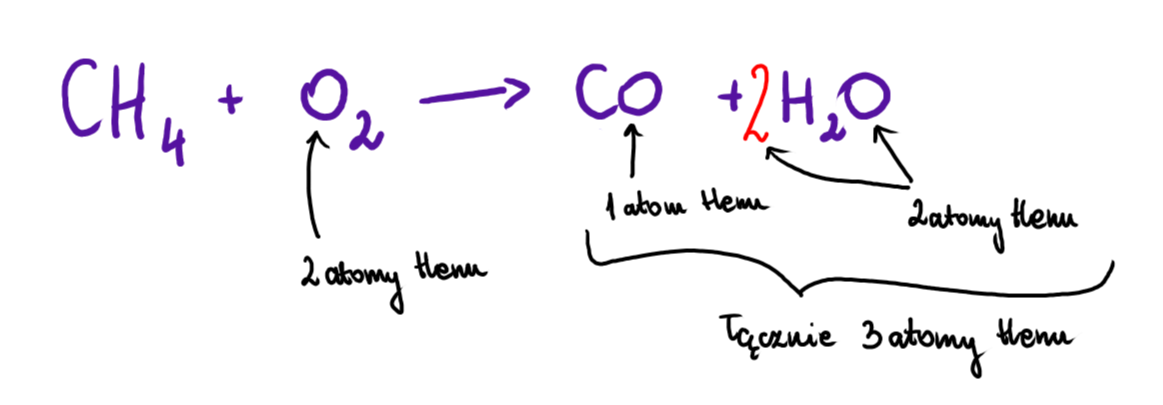REAKCJE SPALANIA ZWIĄZKÓW ORGANICZNYCH
Spalanie wszystkich związków organicznych, odbywa się w identyczny sposób.
Reakcje spalania dzielimy na:
1. spalanie całkowite
2. spalanie niecałkowite (tutaj mamy dwie możliwości)
Napiszmy wszystkie trzy możliwe reakcja spalania dla alkanu o nazwie metan. Wzór sumaryczny tego alkanu to CH4.
Równanie reakcji spalania całkowitego:
Należy teraz dobrać współczynniki stechiometryczne (liczba atomów po lewej stronie równania reakcji chemicznej musi być taka sama jak po stronie prawej):
Liczba atomów węgla (C) po obu stronach równania jest taka sama - super :). Nie zgadza się natomiast liczba wodorów (H) - po lewej stronie jest ich dwa razy więcej niż po prawej. Aby po prawej stronie otrzymać 4 atomy wodoru (czyli dwa razy więcej niż jest teraz), należy całą cząsteczkę wody pomnożyć razy dwa:
Teraz możemy policzyć tlen (O):
Aby po lewej stronie równania również były 4 atomy tlenu, należy dwukrotnie zwiększyć ilość tlenów po stronie lewej:
Zapiszmy teraz równanie reakcji spalania niecałkowitego (pierwsza możliwość). Liczba C i H pozostanie bez zmian, więc od razu zapiszmy 2 przed cząsteczką wody:
Teraz czas na policzenie atomów węgla:
Jeżeli po jednej stronie równania reakcji chemicznej jest parzysta liczba atomów, a po stronie prawej nieparzysta - wówczas przed cząsteczką O2 należy napisać ułamek. W mianowniku tego ułamka będzie zawsze "2", natomiast w liczniku zapisujemy ilość atomów tlenu, które znajdują się po prawej stronie równania reakcji chemicznej:
Na koniec "kosmetyczny" zabieg, który polega na tym aby pozbyć się ułamka - należy pomnożyć całe równanie razy 2:
Otrzymujemy w ten sposób równanie reakcji spalania niecałkowitego, które ma postać:
Na koniec druga opcja spalania niecałkowitego:
Sprawdź czy umiesz poprawnie napisać reakcja spalania dla metanu, etanu, propanu, butanu oraz pentanu:
ALKANY
Tlenki, wodorotlenki, kwasy oraz sole – to związki chemiczne, które tworzą chemię NIEorganiczną. Dzisiaj zaczynamy zupełnie nowy dział – chemię organiczną, której podstawową grupą związków chemicznych są alkany.
Alkany zbudowane są dwóch atomów: węgla czyli C oraz wodoru czyli H. Wartościowość węgla w alkanach jest równa 4, a więc węgiel będzie tworzyć 4 wiązania chemiczne. Natomiast wartościowość wodoru to 1, a więc będzie on tworzył jedno wiązanie chemiczne.
Wiązania chemiczne we wzorach strukturalnych przedstawiamy za pomocą kresek:
Pierwszy alkan o nazwie metan ma jeden atom węgla w swojej cząsteczce:
Atom ten ma cztery wiązania chemiczne:
Atom węgla łączy się za pomocą tych wiązań chemicznych z atomami wodoru:
Świetnie! Narysowaliśmy w ten sposób wzór strukturalny pierwszego alkanu – metanu.
Teraz czas na wzór sumaryczny czyli ten krótki. W tej cząsteczce mamy 1 atom węgla oraz 4 atomu wodoru. Jedynek w chemii nie piszemy, a więc wzór ma postać CH4.
Kolejny alkan ma nazwę etan i tworzą go 2 atomy węgla, które łączymy ze sobą za pomocą jednego wiązania chemicznego:
Teraz należy dorysować kolejne wiązania chemiczne tak, aby każdy węgiel ma łącznie 4 wiązania. Pamiętaj, że wiązania między dwoma węglami oznacza, że każdy atom węgla ma już jedno wiązania, a więc do 4 każdemu brakuje jeszcze 3. W puste miejsca wpisujemy wodory:
Wzór sumaryczny etanu to C2H6.
W chemii mamy jeszcze dwa rodzaje wzorów: wzór półstrukturalny oraz grupowy.
We wzorze półstrukturalnym zapisujemy atomy węgla wraz z wiązaniem chemicznym, które występuje między nimi. Następnie należy dopisać przy atomach węgla - atomy wodoru, które połączone są bezpośrednio z danym węglem. W etanie do pierwszego i drugiego atomu węgla dołączone są po 3 atomy wodoru co zapisujemy jako:
Wzór grupowy jest identyczny jak półstrukturalny, z tą różnicą, że nie zapisujemy w nim wiązania między węglami:
Kolejny alkan to propan, który ma 3 atomy węgla w cząsteczce. Wzór strukturalny przyjmuje więc postać:
Wzór sumaryczny propanu to C3H8.
Wzór półstrukturalny to 3 atomy węgla oraz brakujące atomy wodoru, które przy pierwszym węglu są 3, przy drugim 2 a przy 3 – 3:
Nie zapominaj o wzorze grupowym:
Kolejny alkan to butan, który ma 4 atomy węgla w cząsteczce:
Jeżeli grupy CH2 we wzorze półstrukturalnym powtarzają się obok siebie, wówczas możemy skrócić ten wzór do postaci (grupę CH2 umieszczamy w nawiasie a za nawiasem zapisujemy ile jest takich samych grup i w tym przypadku mamy 2 grupy CH2):
Kolejne alkany mają nazwy:
Pentan – który ma 5 atomów węgla w cząsteczce, a jego wzór sumaryczny to C5H12
Heksan – który ma 6 atomów węgla w cząsteczce, a jego wzór sumaryczny to C6H14
Heptan – który ma 7 atomów węgla w cząsteczce, a jego wzór sumaryczny to C7H16
Oktan – który ma 8 atomów węgla w cząsteczce, a jego wzór sumaryczny to C8H18
Nonan – który ma 9 atomów węgla w cząsteczce, a jego wzór sumaryczny to C9H20
Dekan – który ma 10 atomów węgla w cząsteczce, a jego wzór sumaryczny to C10H22
Wzór ogólny alkanów ma postać:
CnH2n+2
gdzie n to liczba atomów węgla. Natomiast liczba atomów wodoru jest równa 2*n+2 (2 razy n dodać 2)
ALKENY
Alkeny w swojej cząsteczce mają jedno wiązanie podwójne pomiędzy atomami węgla, które zaznaczamy w następujący sposób:
C=C
Pamiętać należy o tym, że węgiel (tak jak w przypadku alkanów) jest czterowartościowy, a więc będzie on tworzył cztery wiązania chemiczne (4 łapki).
Nazwy alkenów, tworzymy od nazw alkanów, zmieniając ich końcówkę z -en na -an.
W przypadku alkanu o nazwie metan, który ma jeden atom węgla w swojej cząsteczce, nie będzie on miał swojego odpowiednika w formie alkenu. Jest to związane z tym, że w alkenach występuje wiązanie podwójne między dwoma atomami węgla. Metan ma tylko jeden atom węgla, a więc nie może on stworzyć wiązania podwójnego.
Pierwszym alkenem będzie zatem alken pochodzący od etanu. Jego nazwa to eten. Ma on w swojej cząsteczce dwa atomy węgla (tak jak w przypadku alkanu), pomiędzy którymi występuje jedno wiązanie podwójne:
Każdy atom węgla musi mieć po 4 wiązania chemiczne. Na powyższym rysunku, każdy atom węgla ma już dwa wiązania, a więc do czterech brakuje im jeszcze po dwa wiązania chemiczne, które utworzą z atomami wodoru:
Powyższy wzór nazywamy wzorem strukturalnym. Wzór sumaryczny ma postać C2H4. Oprócz wzoru strukturalnego i sumarycznego, możemy zapisać również wzór półstrukturalny oraz grupowy:
Kolejny alken pochodzi od propanu, który w swojej cząsteczce ma 3 atomy węgla.
Między 1 i 2 węglem należy zaznaczyć wiązanie podwójne. Nazwa tego alkenu to propen.
Teraz czas na wodory. Pierwszy węgiel ma już dwa wiązania chemiczna, a więc do czterech brakuje mu jeszcze dwóch. Drugi węgiel ma już trzy wiązania chemiczne (dwa na lewo i jeden na prawo), a więc do czterech brakuje mu jeszcze jednego. Trzeci węgiel ma jedno wiązanie, a więc brakuje mu jeszcze trzech:
Powyższy wzór nazywamy wzorem strukturalnym. Wzór sumaryczny ma postać C3H6.
Pozostałe wzory można zapisać jako:
Poniżej dwa kolejne przykłady: buten oraz penten:
Wzór ogólny alkanów ma postać:
CnH2n
gdzie n to liczba atomów węgla. Natomiast liczba atomów wodoru jest równa 2*n (2 razy n)